BADANIE WPŁYWU WYBRANYCH ESTRÓW KWASÓW DIKARBOKSYLOWYCH NA ZUŻYCIE UKŁADU TARCIOWEGO STAL-STAL
THE EFFECT OF SELECTED DICARBOXYLIC ACID ESTERS ON WEAR OF THE STEEL-ON-STEEL MATING ELEMENTS
Czesław KAJDAS, Mohamed AL-NOZILI, Ewa KĘDZIERSKA, Krystyna KARDASZ
Politechnika Warszawska, WBMiP, Instytut Chemii w Płocku
Słowa kluczowe: dodatki przeciwzużyciowe, mechanizm działania dodatków, estry kwasów dikarboksylowych, tribopolimeryzacja, połączenia chelatowe, tribochemia
Publikowane w: TRIBOLOGIA, nr 3, 1998, s. 339
Streszczenie
Wykonano syntezy oraz zbadano właściwości tribologiczne mono i diestrów różnych kwasów dikarboksylowych w celu wyjaśnienia mechanizmu ich działania przeciwzużyciowego. Zakładano, że możliwe jest wystąpienie trzech rodzajów mechanizmów. Estry mogą ulegać: tribopolikondensacji (tribopolimeryzacji), adsorpcji na powierzchni z utworzeniem soli żelazowej kwasu karboksylowego (mydła) oraz tworzyć wiązania chelatowe z metalem powierzchni. Uzyskane wyniki wykazały, że efektywność działania tych dodatków nie może być przypisana tylko jednemu z rozważanych mechanizmów.WPROWADZENIE
Spośród licznej gmpy estrów kwasów dikarboksylowych niektóre są znane jako syntetyczne oleje bazowe, niektóre zaś wykazują właściwości dodatków przeciwzużyciowych.CEL I TEZA PRACY
Przegląd literatury wyraźnie wskazuje na niekompletność danych potwierdzających proces tribopolikondensacji, w szczególności w odniesieniu do układu tarciowego stal-stal. Zatem celem tej pracy jest zbadanie trzech różnych grup funkcyjnych występujących w monoestrach kwasu dikarboksylowego i glikoli oraz ich roli w działaniu przeciwzużyciowym tych związków, przy uwzględnieniu różnych mechanizmów ich działania. Tak zaplanowany cel badań wynika z postawionej tezy pracy mówiącej, że bardzo dobre właściwości przeciwzużyciowe tego typu dodatków mogą być związane (oprócz wymienionych wyżej mechanizmów: tribopolikondensacji i tworzenia mydeł) również z oddziaływaniem grup funkcyjnych z powierzchnią, w szczególności zaś grupy estrowej będącej w bliskim sąsiedztwie grupy hydroksylowej. Ugrupowanie takie powinno tworzyć specyficzny i trwały film smarowy poprzez odpowiednie układy chelatowe z metalem powierzchni. Do badań wybrano estry, których budowa w połączeniu z charakterystyką przeciwzużyciową mogłyby dostarczyć informacji wskazujących na udział różnych mechanizmów działania dodatków. Ponadto zbadano estry zawierające wiązanie podwójne w celu rozważenia ewentualnego udziału tribopolimeryzacji typu winylowego (ponieważ monoester kwasu dikarboksylowego C35 i glikolu etylenowego zawiera wiązanie nienasycone).CZĘŚĆ DOŚWIADCZALNA
Substancje smarowe
Zgodnie z założeniem niniejszej pracy, do badań wybrano sześć różnych estrów, których budowa chemiczna może wyraźnie różnicować ich mechanizm działania przeciwzużyciowego. Nazwy i wzory strukturalne tych estrów, łącznie z opisem zakładanego mechanizmu ich działania zestawiono w TABELI l.
Tabela 1 | |||||||||||
| Nazwa i wzór uproszczony | Skrót nazwy | Zakładany mechanizm działania | |||||||||
| 1 | Monoester kwas oktanodiowy - glikol 1,2-heksadekanowy HOOC—(CH2)6—COOCH2CHOH(CH2)13CH3 | MEDOG | Reakcja z powierzchnią poprzez grupę —COOH oraz reakcja polikondensacji w wyniku międzycząsteczkowej reakcji grup —COOH z grupami —OH | ||||||||
| 2 | Monoester kwas oktanodiowy - alkohol C18 HOOC—(CH2)6—COOCH2(CH2)16CH3 | MEDOA | Reakcja z powierzchnią poprzez grupę —COOH | ||||||||
| 4 | Diester kwasu maleinowy - alkohol C18 CH3(CH2)16CH2OOC(CH2)COOCH2(CH2)(CH2)16CH3 | DEMAL | Tribopolimery- zacja addycyjna. | Adsorpcja na powierz- chni poprzez niewiążące pary elektronów tlenu w grupach estrowych; zakładana jest różnica w zależności od izomerii cis-trans i konformacji | |||||||
| 5 | Diester kwas furnarowy - alkohol C18 CH3(CH2)16CH2OOC(CH?)2COOCH2(CH2)16CH3 | DEFUM | |||||||||
| 6 | Diester kwas bursztynowy - alkohol C18 CH3(CH2)16CH2OOC(CH2)2COOCH2(CH2)16CH3 | DEBUR | |||||||||
Warunki prowadzenia testów tribologicznych Ocenę właściwości przeciwzużyciowych estrów przeprowadzono za pomocą tribometru tarcza-trzpień (TESTER T-01M produkcji Zakładu Tribologii w Instytucie Technologii Eksploatacji w Radomiu) [L. 13].
Tabela 2 | |||||||||||
| Układ testujący | Warunki prowadzenia testów | ||||||||||
| Układ materiałowy | stal-stal | ||||||||||
| Geometria układu | kulka na płaszczyźnie (umocowana na stałe kulka ślizgająca się po obracającej się tarczy) | ||||||||||
| Charakterystyka pary tribologicznej | kulka ze stali ŁH15 o średnicy 0,315 mm, produkcji Zakładów Łożysk Tocznych „Iskra” w Kielcach; dysk ze stali ŁH15 o średnicy 25,4 mm, grubości 7 mm | ||||||||||
| Sposób smarowania | smarowanie zanurzeniowe | ||||||||||
| Dystans | 500 m | ||||||||||
| Prędkość | 0.25 m/s | ||||||||||
| Obciążenie | l, 2 lub 3 kG | ||||||||||
gdzie:
WYNIKI BADAŃ
Charakterystyka chemiczna badanych estrów
Cząsteczka monoestru kwasu oktanodiowego i l ,2-heksadekanodiolu (MEDOG) zawiera wolną grupę karboksylową oraz hydroksylową; istnieje zatem potencjalna możliwość przebiegu reakcji polikondensacji intermolekularnej. Jednocześnie obecność niewiążących par elektronowych na atomach tlenu w ww. grupach oraz w grupie estrowej pozwala teoretycznie zarówno na adsorpcję na powierzchni, jak i tworzenie mydeł (dla grupy karboksylowej).
 |
|
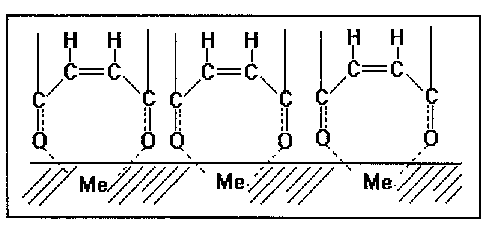
Rys. l. Zakładany mechanizm sorpcji diestru kwasu maleinowego na powierzchni metalu Fig. l. Assumed sorption mechanism of the ester ofmaleinic acid on the metal surface |
 |
|
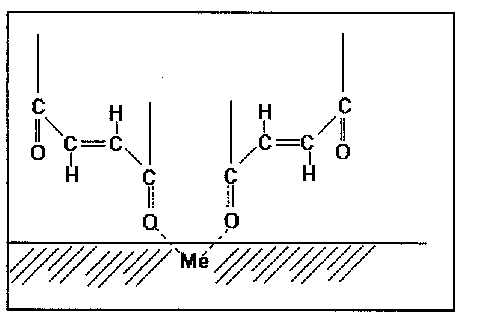
Rys. 2. Zakładany mechanizm sorpcji diestru kwasu fumarowego na powierzchni metalu Fig. 2. Assumed sorption mechanism of the ester offumaric acid on the metal surface |
 |
|
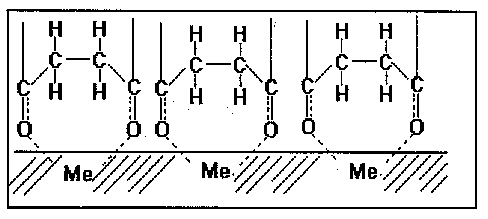
Rys. 3. Zakładany mechanizm sorpcji diestru kwasu bursztynowego na powierzchni metalu Fig. 3. Assumed sorption mechanism of the ester of succinic acid on the metal surface |
Właściwości przeciwzużyciowe badanych estrów
Wyniki badań przeciwzużyciowych wszystkich estrów w stężeniu 0,01; 0.1 i 1% (m/m), przy trzech różnych obciążeniach, zestawiono w TAB. 3. Ze względu na bardzo małą rozpuszczalność estru MEDOG w n-heksadekanie, ester ten nie był badany w stężeniu 1%. Dla każdego roztworu wykonano 5 testów; odchylenia standardowe są umieszczone w TAB. 4
Tabela 3 | |||||||||||
| Rodzaj związku | Redukcja zużycia kulki [%] | ||||||||||
|
Obciążenie, 1 kG Stężenie [%] | Obciążenie, 2 kG Stężenie [%] | Obciążenie, 3 kG Stężenie [%] | |||||||||
| 0,01 | 0,1 | 1 | 0,01 | 0,1 | 1 | 0,01 | 0,1 | 1 | |||
| Bez dodatku | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | ||
| MEDOG | 82 | 88 | * | 55 | 85 | * | 53 | 84 | * | ||
| MEDOA | 89 | 73 | 88 | 60 | 70 | 71 | 57 | 66 | 62 | ||
| MEC36G | 60 | 90 | 56 | 54 | 87 | 56 | 52 | 86 | 55 | ||
| DEFUM | 0 | 0 | 55 | 0 | 5 | 49 | 10 | 13 | 48 | ||
| DEMAL | 6 | 21 | 74 | 21 | 31 | 61 | 22 | 35 | 58 | ||
| DEBUR | 0 | 18 | 73 | 18 | 26 | 60 | 18 | 33 | 57 | ||
| * związek nie rozpuścił się w n-heksadekanie | |||||||||||
Tabela 4 | |||||||||||
| Rodzaj związku | Odchylenie standardowe | ||||||||||
|
Obciążenie, 1 kG Stężenie [%] | Obciążenie, 2 kG Stężenie [%] | Obciążenie, 3 kG Stężenie [%] | |||||||||
| 0,01 | 0,1 | 1 | 0,01 | 0,1 | 1 | 0,01 | 0,1 | 1 | |||
| MEDOG | 1,7 | 1,1 | * | 2,2 | 3,4 | * | 4,3 | 4,2 | * | ||
| MEDOA | 2,4 | 4,5 | 0,9 | 3,8 | 2,2 | 2,7 | 4,5 | 4,8 | 4 | ||
| MEC36G | 5,34 | 1,9 | 3,0 | 2,5 | 2,2 | 4,2 | 4,1 | 4,1 | 4,8 | ||
| DEFUM | 2,70 | 9,2 | 3 | 4,40 | 4,5 | 8,5 | 3,5 | 5,3 | 4,7 | ||
| DEMAL | 1,7 | 4,9 | 3,43 | 2,9 | 3 | 3 | 3 | 2,4 | 4.4 | ||
| DEBUR | 4,3 | 4,2 | 3,1 | 5,24 | 3,77 | 2,77 | 3,2 | 4,9 | 3,56 | ||
OMÓWIENIE WYNIKÓW BADAŃ I WNIOSKI
Obciążenie 1kG
a. Monoestry
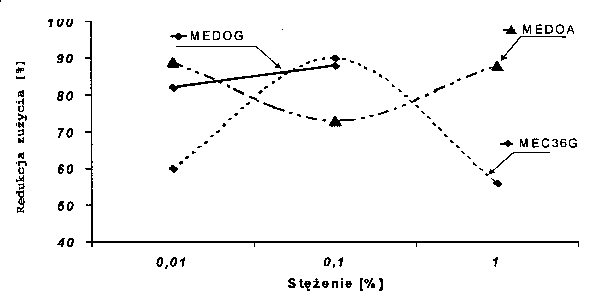
Efektywność działania monoestru kwasu dikarboksylowego C36 i 1,2-etanodiolu (MEC36G), opisywanego w literaturze jako dodatku działającego według mechanizmu tribopolikondensacji, zależy w znacznym stopniu od użytego stężenia. Najefektywniejsze działanie przeciwzużyciowe (redukcja zużycia materiału o 90%) zaobserwowano przy stężeniu 0.1% (RYS. 4).
 |
|
Rys. 4. Redukcja zużycia kulki spowodowana działaniem badanych monoestrów (obciążenie 1kG) Fig. 4. The ball wear reduction caused by action of used monoesters (load: l kG) |
b. Diestry
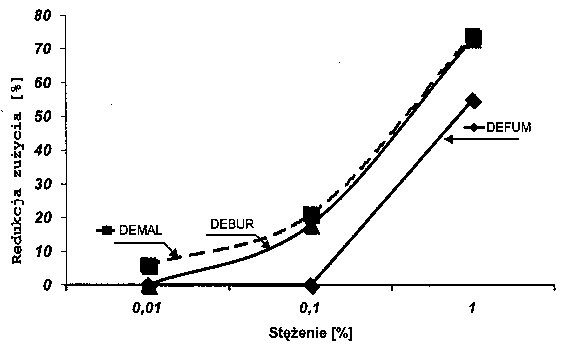
Efektywność działania przeciwzużyciowego wszystkich diestrów wzrasta wraz ze wzrostem stężenia. W przypadku tych związków brak wolnych grup karboksylowych i hydroksylowych wyklucza przebieg reakcji polikondensacji, teoretycznie możliwa jest jednak reakcja polimeryzacji addycyjnej w przypadku diestrów kwasów maleinowego (DEMAE) i fumarowego (DEFUM), ze względu na obecności podwójnego wiązania (RYS. 5).
 |
|
Rys. 5. Redukcja zużycia kulki spowodowana działaniem badanych diestrów (obciążenie 1kG) Fig. 5. The ball wear reduction caused by action of used diesters (load: 1 kG) |
Obciążenie 2 kG
a. Monoestry
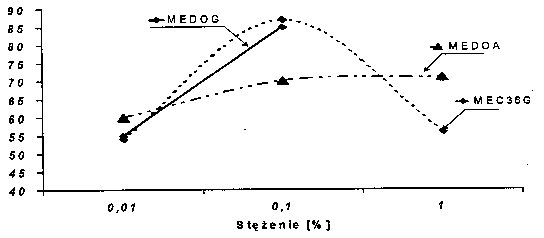
Monoester kwasu dikarboksylowego C36 i 1,2-etanodiolu (MEC36G). przy tym obciążeniu zachowuje podobną zależność efektywności od stężenia jak przy obciążeniu l kG. Monoester kwasu oktanodiowego i 1,2--heksadekanodiolu (MEDOG) wykazuje porównywalne właściwości przeciwzużyciowe do MEC36G zarówno w stężeniu 0.01%, jak i 0.1%. Natomiast MEDOA w stężeniu 0,01 % i 1% jest bardziej efektywny niż MEC36G, co może świadczyć o uprzywilejowaniu reakcji z powierzchnia w tych stężeniach, podczas gdy przy stężeniu 0,1% zaznacza się wpływ reakcji tribopolikondensacji (RYS. 6).
 |
|
Rys. 6. Redukcja zużycia kulki spowodowana działaniem badanych monoestrów (obciążenie 2 kG) Fig. 6. The ball wear reduction caused by action ofused monoesters (load: 2 kG) |
b. Diestry
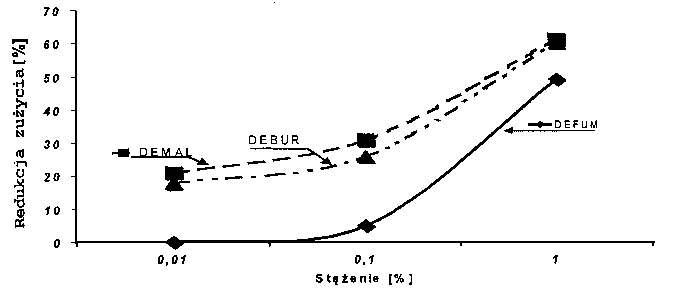
Również przy tym obciążeniu efektywność wszystkich trzech diestrów wzrasta wraz ze wzrostem stężenia, przy czym w porównaniu z obciążeniem l kG obserwowano wzrost efektywności działania przy niższych stężeniach (0.01 i 0.1%) z jednoczesnym spadkiem efektywności działania przy stężeniu 1% (RYS. 7). Gorsza efektywność diestru kwasu fumarowego (DEFUM) w zestawieniu z nieco większą efektywnością diestrów kwasów maleinowego (DEMAE) i bursztynowego (DEBUR) z jednoczesnym niewielkim zróżnicowaniem wartości redukcji zużycia pomiędzy diestrem kwasu maleinowego i bursztynowego (redukcja zużycia odpowiednio: 21-61 i 18-60%) może świadczyć, że udział reakcji polimeryzacji addycyjnej jest niewielki lub żaden. Uzyskany efekt przeciwzużyciowy jest prawdopodobnie wynikiem adsorpcji cząsteczek na powierzchni metalu za pośrednictwem niewiążących par elektronowych na atomach tlenu grup estrowych.
 |
|
Rys. 7. Redukcja zużycia kulki spowodowana działaniem badanych diestrów (obciążenie 2 kG) Fig. 7. The ball wear reduction caused by action of used diesters (load: 2 kG) |
Obciążenie 3 kG
a. Monoestry
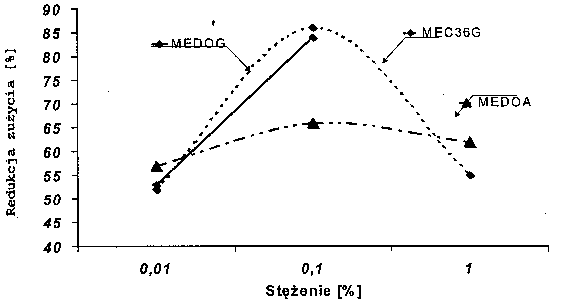
Monoester kwasu dikarboksylowego C36 i 1,2-etanodiolu (MEC36G), oraz monoester kwasu oktanodiowego i 1,2-heksadckanodiolu (MEDOG) zachowały się identycznie jak przy obciążeniu 2 kG, natomiast obserwowano dalszy spadek efektywności działania monoestru kwasu oktanodiowego i oktadekanolu (MEDOA); można zatem wnioskować, że przy tym obciążeniu większy jest wpływ polikondensacji (RYS. 8).
 |
|
Rys. 8. Redukcja zużycia kulki spowodowana działaniem badanych monoestrów (obciążenie 3 kG) Fig. 8. The ball wear reduction caused by action of used monoesters (load: 3 kG) |
 |
|
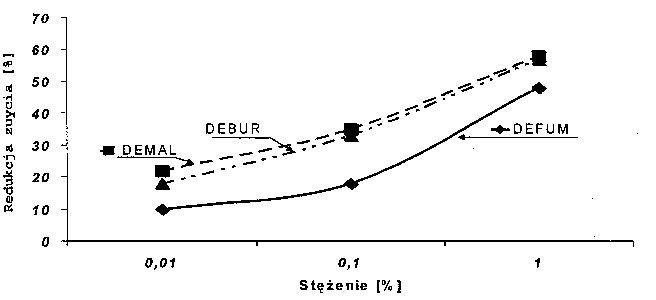
Rys. 9. Redukcja zużycia kulki spowodowana działaniem badanych diestrów (obciążenie 3 kG) Fig. 9. The ball wear reduction caused by action ofused diesters (load: 3 kG) |
PODSUMOWANIE
-
Uzyskane wyniki badań pozwalają na sformułowanie następujących wniosków:
- Efektywności przeciwzużyciowej estrów nie można uzasadnić istnieniem jednego mechanizmu, wspólnego dla wszystkich badanych związków.
- Udział poszczególnych mechanizmów działania estrów w ostatecznym efekcie przeciwzużyciowym zmienia się zarówno w zależności od zastosowanego stężenia, jak i obciążenia.
- W badanych warunkach najefektywniejsze są estry, których działanie można przypisać zarówno reakcji z powierzchnią, jak i wiązać z ewentualnym występowaniem mechanizmu tribopolimeryzacji.
- Porównanie wyników badań diestrów kwasów fumarowego, maleinowego i bursztynowego wskazują na słuszność postawionej tezy dotyczącej tworzenia układów chelatowych.
LITERATURA
- Shubkin, R.L.: Synthetic lubricants and high performance functional fluid. Marcel Dekker, Inę. New York, Basel, Hong Kong 1993.
- Bartz W.J.: Comparison of Synthetic Fluids. Lub. Eng., 48 (1992), s. 765-774.
- Furey M.J.: The Formation of Polymeric Films Directly on Rubbing Surfaces to Reduce Wear. Wear, 26, 369-92, 1973.
- Kempiński R., Kędzierska E., Kardasz K., Konopka M., Wilkanowicz L.: Dodatki tribologiczne działające według mechanizmu tribopolimeryzacji. Część III, Tribologia, 1996, 6, s. 700-721.
- Furey M.J., Kajdas C., Ward T.C.: Hellgeth J.W.: Thermal and Catalytic Effects on Tribopolymerization as a New Boundary Lubrication Mechanism. Plenary Lecture 5th International Congress on Tribology, Helsinki, Finland, June 12-15, 1989; także publikowane w Wear, 136, 85-97, 1990.
- Kajdas C., Lafleche P.M., Furey M.J., Hellgeth J.W, Ward T.C.: A Study of Tribopolymerization under Fritting Contact Conditions. 8th International Colloquium Tribology 2000, Eslingen, 14-16 January 1992, 8.4-1 - 8.4-13.
- Furey M.J., Kajdas C.: Tribopolimeryzation as a novel approach to ceramic lubrication. in Proc. 4th Int. Sym. On Ceramic Materials and Componcnts for Engines, R. Carlsson, T. Johnansson, and L. Kahiman (eds.), Elsevier Applicd Science, London, 1992, pp. 1211-18.
- Furey M.J., Ghasemi H., Tripathy B.S., Kajdas C., Kempiński R., Hellgeth J.W.: Tribochemistry of the Antiwear Action of Dimer Acid/glycol Monoester on Aluinina. STEL Prepint 93-AM-6E-1, 1993.
- Masuko M., Ohmori T., Okabe H.: Anti-wear Propertics of Hydroxycarboxylic Acids with Straight Alkyl Chains. Tribology International August Vol.21 No 4, 1988, 199-203.
- Okabe H., Minami I., Kitamura H., Masuko M.: 2-Hydroxycarboxylic Acid as Novel Friction-polymer Type Additives. JSLE International Tribology Conference, Nagoya, Japan, Oct. 29-Nov. l, 1990, 1049-1054.
- Kąjdas C., Furey M.J., Kempiński R.: Tribopolimeryzation: II. NIRAM Applications to the Antiwear Action of Addition-Type Monomers. Proceedings of the 2nd Symposium 15-17 September 1997, Janowice, Poland, pp. 127-139.
- Furey M.J., Kąjdas C., Kempiński R.: Tribopolimeryzation: Surface Temperatures and the Antiwear Action of Condensation-Type Monomers. Proceedings of the 2nd Symposium 15-17 September 1997, Janowice, Poland. pp.115-125.
- Kempiński R., Kędzierska E., Kardasz K., Konopka M., Wilkanowicz L.: Dodatki tribologiczne do olejów działające według mechanizmu tribopolimeryzacji. Część I. Tribologia 1995, 3, s. 277-298.
Recenzent: Marian Włodzimierz SUŁEK
Summary
Syntheses and tribological properties of different mono and diesters of dicarboxylic acids were performed in order to explain the mechanism of their antiwear activity. There are supposed three possible mechanisms: tribopolycondensation (or tribopolymerization), adsorption and forming „soaps” in reaction with surface metal. Effectiveness of the esters was investigated with pin-on-disc device on steel-steel system. Analysis of obtained results showed that:- it is impossible to explain the antiwear effectiveness of the tested compounds with only one mechanism:
- participation of each of mentioned above mechanisms changes in relation to concentration and load.
- the most effective are the esters for which mechanisms both tribopolycondensation and forming „soaps" are possible.
- comparison of results for diesters of following acids: fumaric, maleic and succinic shows that thesis of chelate forming is probably correct.